Życie, to współpraca mikroskopijnych łańcuchów:
Znalazłem na youtube świetną animację syntazy ATP, co skłoniło mnie do napisania tego posta:
1. Kwasów deoksyrybonukleotydowych (DNA):
Znalazłem na youtube świetną animację syntazy ATP, co skłoniło mnie do napisania tego posta. Życie, to współpraca mikroskopijnych łańcuchów:
Replikacja DNA (polski lektor):
![]()


Polimeraza DNA
Polimeraza DNA. Enzym ten ma zdolność usuwania błędów, jak się pomyli podczas kopiowania materiału genetycznego:

Za kompleksem replikacyjnym podążają wyspecjalizowane kompleksy molekularne, by poprawiać to, co przeoczyła polimeraza DNA! Poza tym ten typ polimerazy naprawia tylko jedną nić. Podczas replikacji Dna uczestniczą dwie polimerazy:
https://pl.wikipedia.org/wiki/Naprawa_DNA
„Naprawa DNA – szereg procesów prowadzących do identyfikacji i naprawy zmian w cząsteczkach DNA w żywej komórce. W komórkach organizmów żywych procesy metaboliczne i czynniki środowiskowe mogą powodować uszkodzenie DNA. W każdej komórce codziennie ma miejsce nawet milion takich uszkodzeń. Wiele z nich powoduje trwałe zmiany w cząsteczce DNA, które mogą upośledzić albo pozbawić komórkę możliwości prawidłowej transkrypcji kodowanego przez uszkodzony fragment DNA genu. Inne uszkodzenia mogą skutkować potencjalnie groźną dla genomu komórki mutacją, dotyczącą tej komórki i wszystkich następnych powstałych z niej po podziałach. Oznacza to, że proces naprawy DNA w komórce musi być cały czas aktywny, by móc szybko i skutecznie niwelować skutki każdego uszkodzenia komórkowego DNA.
Powodzenie naprawy DNA zależy od wielu czynników, w tym typu i wieku komórki oraz środowiska pozakomórkowego. W komórce, w której duża ilość DNA uległa uszkodzeniu albo której mechanizmy naprawy DNA nie są wystarczająco efektywne, mogą zajść:
- nieodwracalny stan wygaśnięcia aktywności komórki – starzenie się komórki;
- samobójcza śmierć komórki, czyli apoptoza;
- niekontrolowane podziały, prowadzące do powstania nowotworu.
Zdolność komórki do naprawy własnego DNA jest istotna dla integralności fizycznej całego genomu oraz integralności informacji genetycznej, którą niesie, a więc i dla prawidłowego funkcjonowania całego organizmu. Wiele genów które początkowo zidentyfikowano jako wpływające na długość życia komórek, z czasem okazały się być zaangażowane w procesy naprawy i ochrony DNA przed uszkodzeniem. Nieprawidłowy przebieg naprawy zniszczeń komórkowych w komórkach generatywnych może doprowadzić do propagacji mutacji w gametach i w rezultacie, przekazania mutacji potomstwu. Z drugiej strony, między innymi takie mutacje są siłą napędową ewolucji biologicznej.„
http://www.e-biotechnologia.pl/artykuly/naprawa-dna
Naprawa DNA pośrednia
BER (ang. base excision repair) – koryguje niewielkie uszkodzenia poprzez wycinanie i naprawianie pojedynczych zasad, które uległy modyfikacjom chemicznym (np. alkilacji, deaminacji). Proces ten zachodzi etapowo:
• Odpowiednia glikozydaza DNA przecina wiązanie β-N-glikozydowe, a następnie usuwa uszkodzoną zasadę tworząc miejsce AP (apurynowe lub apirymidynowe).
• Wiąże się do nich polimeraza DNA I (Pol I), która następnie wypełnia lukę nową nicią syntetyzowaną na martycy DNA. U różnych organizmów w procesie tym biorą udział różne rodzaje polimerazy.
• Na koniec ligaza DNA łączy obie nici i syntetyzuje ostatnie wiązanie fosfodiestrowe.
Niektóre glikozydazy wykazują dodatkową aktywność nukleolityczną. Nacinają one łańcuch po stronie 3’ miejsca AP i tworzą jednonukleotydową lukę w DNA.
Naprawa typu NER
Globalna naprawa genomu NER – GGR (ang. global genomie repair) dotyczy nici DNA nie ulegające transkrypcji i odbywa się stosunkowo wolno.
Geny podlegające aktywnej transkrypcji naprawiane są dzięki mechanizmowi NER-TCR (ang. transcription-coupled repair), a ich uszkodzenia rozpoznaje Polimeraza RNA.
Należy pamiętać, że te skomplikowane procesy na animacjach pokazano w bardzo dużym uproszczeniu. W rzeczywistości biorą w nich udział maszyny precyzyjnie, utkane z łańcuchów złożonych z połączonych aminokwasów w ściśle określonej sekwencji! Na poniższej animacji bardziej realistycznie pokazano proces naprawy DNA – choć to i tak wierzchołek góry lodowej, co zostanie wykazane w dalszej części niniejszego tekstu:
Biolodzy badający i opisujący ten proces bardzo trafnie nazwali to białko:

Na filmie poniżej przedstawiono moc interferencji połączonej z różnymi procesami odpowiedzialnymi za naprawę uszkodzonego DNA w celu chronienia nas przed chorobami genetycznymi, w tym nowotworowymi. Jak bardzo muszą nas truć, i my sami siebie, skoro nowotwory potrafią być szybsze od tych molekularnych maszynerii, które nieustannie przeszukują nasze genomy w celu leczenia skutków ”ucywilizowania” Homo sapiens! Rekombinacja homologiczna, jest ważnym procesem naprawczym. Jednak w guzach nowotworowych zauważono niedobory tych kompleksów z powodu defektu BRCA! Mutacje są tak szybko indukowane w naszych organizmach i tyle ich dziedziczymy po naszych przodkach, że ofiarami padają nawet nasi molekularni sojusznicy 😦
Naprawa błędnie sparowanych nukleotydów
Niekomplementarne nukleotydy rozpoznawane są przez odpowiednie białka (Mut-S, Mut- H i Mut- L u Procaryota, białka kodowane przez geny hMLH i hMSH2 u Eucaryota). Identyfikacja nowo zsyntetyzowanej nici możliwa jest dzięki metyzacji oraz nieobecności połączeń między tworzącymi ją fragmentami Okazaki. Helikaza rozplata podwójną helisę, a egzonukleoaza degraduje oznaczoną nić. Jej fragment wraz z niedopasowanym nukleotydem jest usuwany i odbudowywany przez odpowiednią polimerazę DNA. Ligaza odtwarza wiązania fosfodiestrowe.
U bakterii
Naprawa rekombinacyjna, pozwala na naprawę uszkodzeń występujących w obu niciach (ang. double-strand breaks, DSBs). Jest ona wyjątkowo niebezpieczna dla genomu ze względu na brak matrycy umożliwiającej odtworzenie zmienionego fragmentu.
• Łączenie niehomologicznych końców (ang. non-homologous end joining, NHEJ) – system wykorzystywany do naprawy przerw w przypadku braku homologicznych sekwencji mogących posłużyć do odtworzenia ciągłości nici. Wieloskładnikowy kompleks białkowy kieruje ligazę na miejsce pęknięcia. W jego skład wchodzą: białko Ku, kinaza białkowa DNA-PKCS, białko XRCC4. Mechanizm ten nie jest dokładny, gdyż w uszkodzonym rejonie powstaje kilkunukleotydowa delecja.
Naprawa indukowana, czyli system SOS (ang. save our souls) – ostateczna odpowiedź komórki bakteryjnej na rozległe uszkodzenia DNA. Jest ona regulowana przez wiele operonów i uruchamiana w przypadku pojawienia się jednoniciowego DNA (ssDNA), oligonukleotydów lub wolnych trójfosforanów nukleotydów świadczących o zahamowaniu replikacji. System SOS jest mutagenny. Obniża wierność replikacji DNA i pozostawia błędy w sekwencji nukleotydów.
Najważniejszymi regulatorami systemu SOS są białko RecA (aktywator operonów SOS) i LexA (rep resor wszystkich operonów SOS).
Gdy w komórce nie ma uszkodzeń DNA lub są one na tyle małe, że mogą być naprawione przez inne systemy, cząsteczki białka LexA wiążą się z promotorami operonów SOS hamując ekspresję genów. Łączą się także z promotorem genu RecA. Gdy w komórce pojawią się poważniejsze uszkodzenia, sygnał wysyłany przez ssDNA i ATP powoduje zmianę konformacji białka RecA, które stymuluje autoporteolizę białka LexA i indukcję systemu SOS. W momencie, gdy sygnał o uszkodzeniu DNA zanika, RecA powraca do nieaktywnej konformacji, która nie powoduje już autoprotolizy Lexa:
Inna animacja:




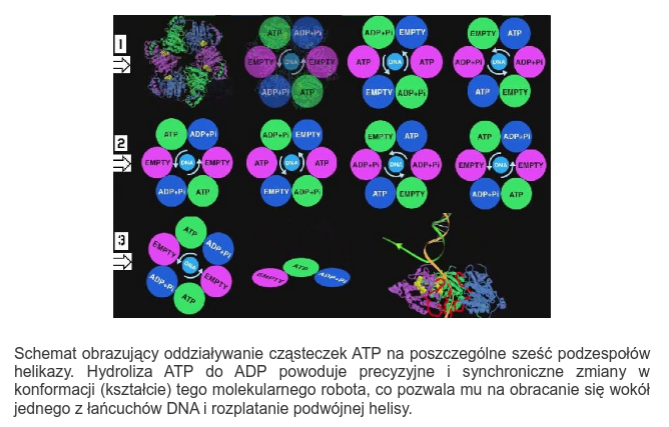

Można by jeszcze dużo o tym pisać, ale pójdę dalej. Wiecie co się dzieje jak łańcuchy DNA zaczynają się naprężać w miarę posuwania się do przodku kompleksu replikacyjnego DNA? Zróbcie proszę eksperyment. Zwiążcie dwa sznurowadła na jednym końcu. Niech imitują dwa łańcuchy DNA, skręcone w podwójną helisę. Jak już je skręcicie, to przywiążcie jeden koniec do klamki i naprężcie helisę. Następnie wsadźcie palca od strony niezwiązanego końca miedzy dwa sznurowadła i przesuwajcie w stronę klamki. Nie da rady dalej niż do połowy? Jest rozwiązanie. przetnijcie blisko klamki jedno sznurowadło i dalej przesuwajcie palec do przodu, a zacznie się odwijać wirując wokół drugiego, przywiązanego do klamki i nie przeciętego. Następnie zwiążcie przecięte i koniec eksperymentu. Dotarliście palcem do klamki, ponieważ sznurowadła uległy relaksacji. Bardzo podobnie dzieje się w żywych komórkach. Jeden z typów enzymów zwanych topoizomerazami, konkretnie topoizomeraza I nacina jedę ą z nici i zachodzi relaksacja i kompleks replikacyjny będzie dalej, inaczej by utknął! 🙂 Następnie przecięta nić zostaje połączona i wszystko jest jak przed zabiegiem. Na animacji pokazano topoizomerazy I i II. Funkcję tej drugiej zaraz omówię, cho ć po obejrzeniu animacji wszystko powinno być jasne. Rozplątuje poplątane łańcuchy DNA!
Schemat działania topoizomerazy I

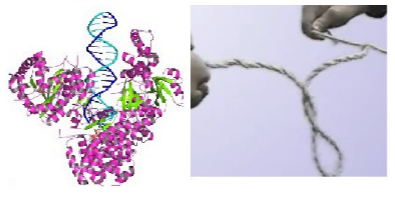
Schematy działania topoizomerazy II

 „Widziałeś filmy, lub bawiłeś się zabawkowymi transformatorami, tymi zmieniającymi kształt maszynami, które zmieniają się w odpowiedzi na każde wyzwanie, przed którym stają? Okazuje się, że molekularne maszyny służące komórce do naprawy DNA potrafią przeobrażać się w podobny sposób podczas walki z rakiem i innymi chorobami. Wniosek wynika z badań prowadzonych przez naukowców z Lawrence Berkeley National Laboratory (Berkeley Lab) z Departamentu Energii USA.”
„Widziałeś filmy, lub bawiłeś się zabawkowymi transformatorami, tymi zmieniającymi kształt maszynami, które zmieniają się w odpowiedzi na każde wyzwanie, przed którym stają? Okazuje się, że molekularne maszyny służące komórce do naprawy DNA potrafią przeobrażać się w podobny sposób podczas walki z rakiem i innymi chorobami. Wniosek wynika z badań prowadzonych przez naukowców z Lawrence Berkeley National Laboratory (Berkeley Lab) z Departamentu Energii USA.”
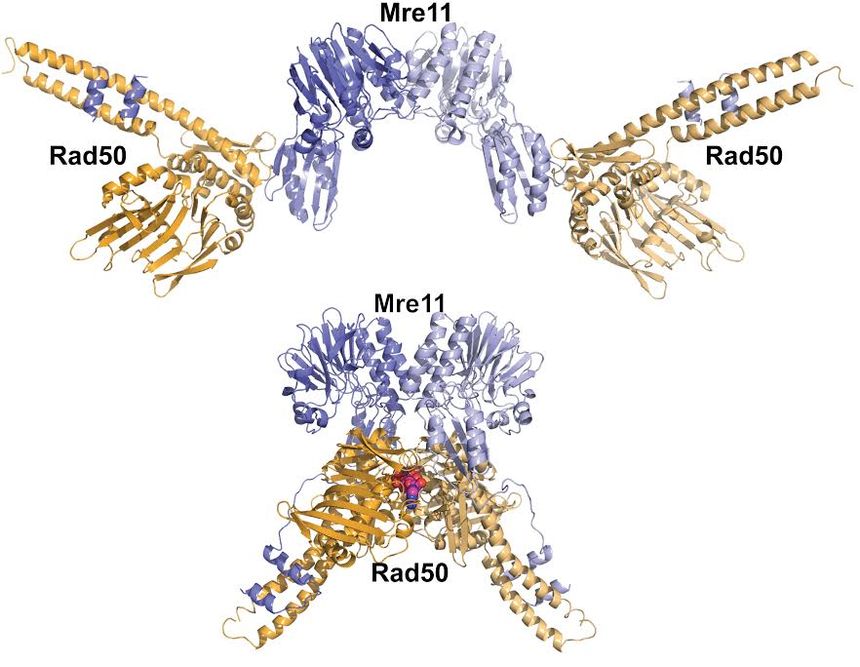
Jak donosi kilka nowych badań, naukowcy uzyskali nowy wgląd w to, jak kompleks białek o nazwie Mre11-Rad50 przekształca się, aby podjąć różne zadania naprawy DNA.
Ich badania rzucają światło na to, w jaki sposób ta restrukturyzacja molekularna prowadzi do różnych wyników w komórce. Może również kierować opracowywaniem lepszych terapii do walki z rakiem i skuteczniejszych terapii genowych.„
How a Shape-shifting DNA-repair Machine Fights Cancer

2. Rybonukleotydowych (RNA):
https://www.smart-biology.com/life-unit-1-from-atoms-to-cells-free-sample-lessons/

Transkrypcja – przepisywanie DNA (genu) na mRNA:


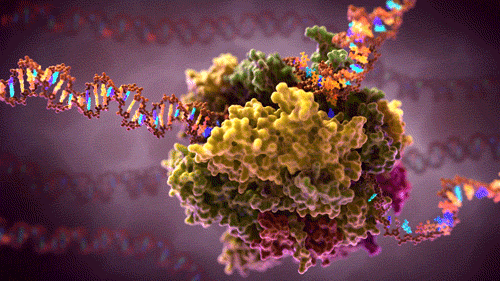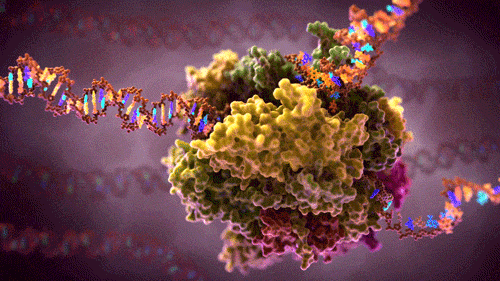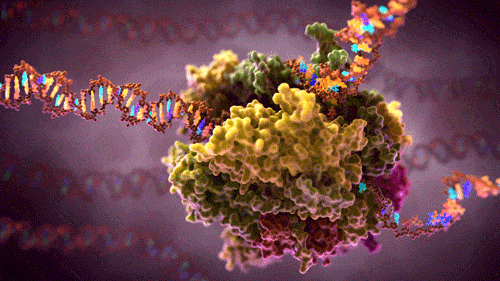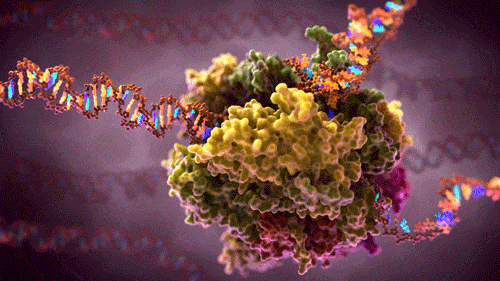
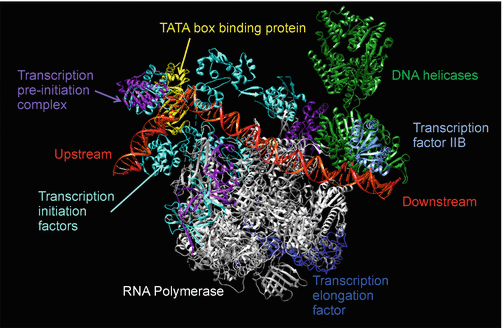
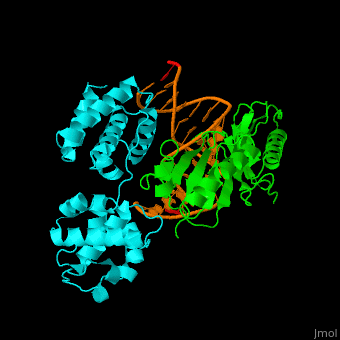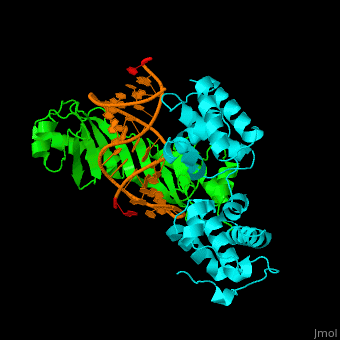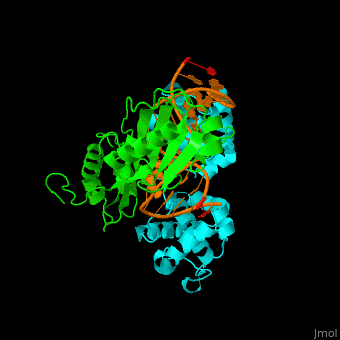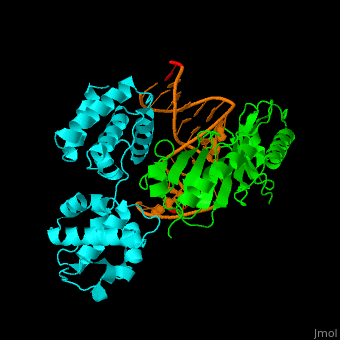
Subtelne i niezbędne dopasowania w biologii molekularnej





Polimeraza RNA. Od polimerazy DNA różni się tym, że nie kopiuje z DNA na DNA, tylko z DNA na mRNA:
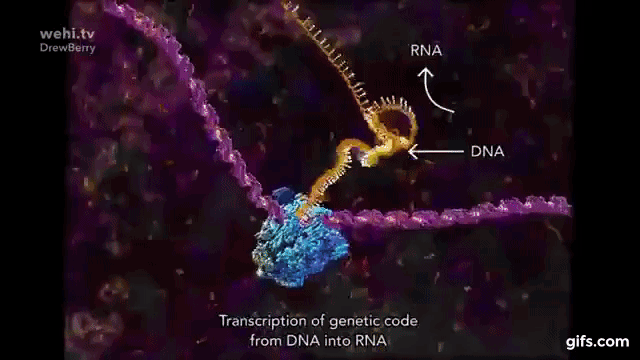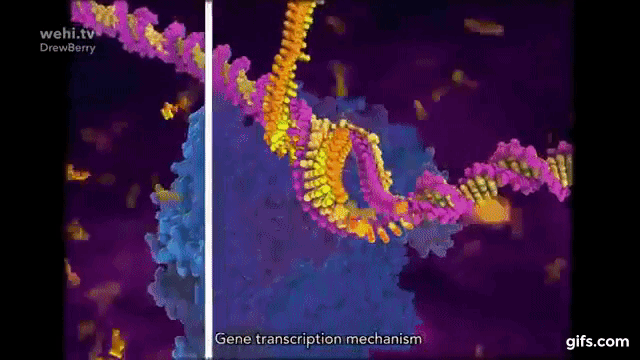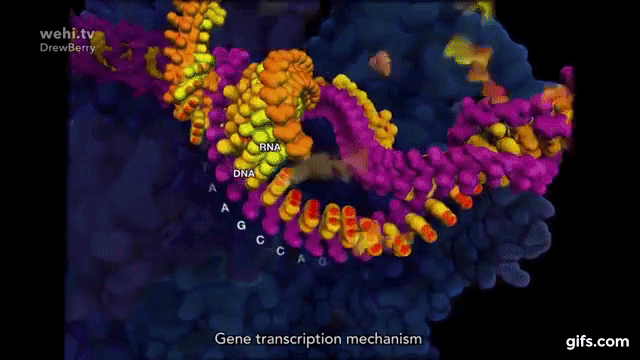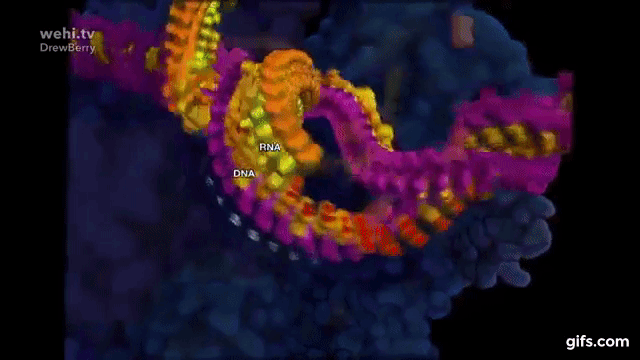

Translacja – synteza białek na matrycy mRNA:
Z polipeptydów (białek):
https://opentextbc.ca/microbiologyopenstax/chapter/proteins/
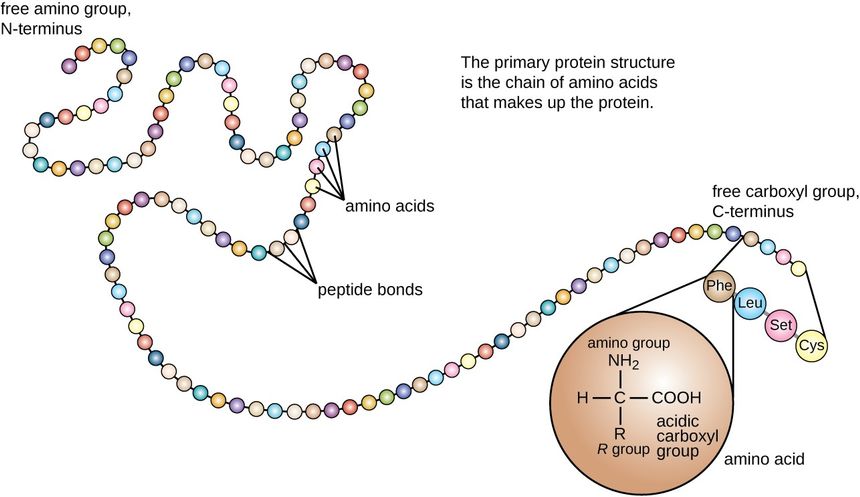





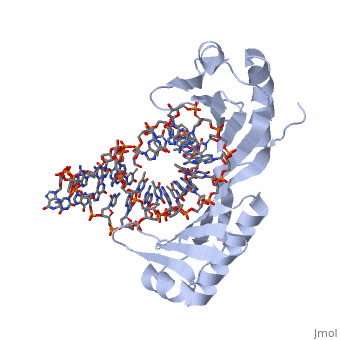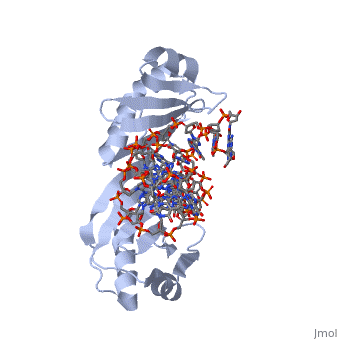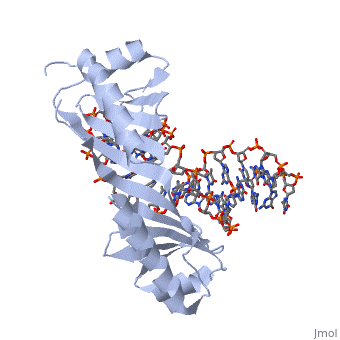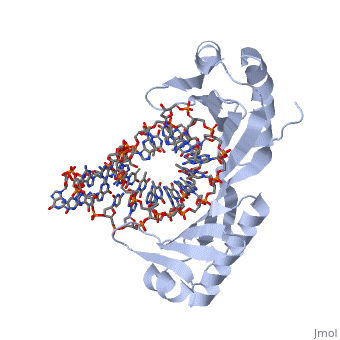





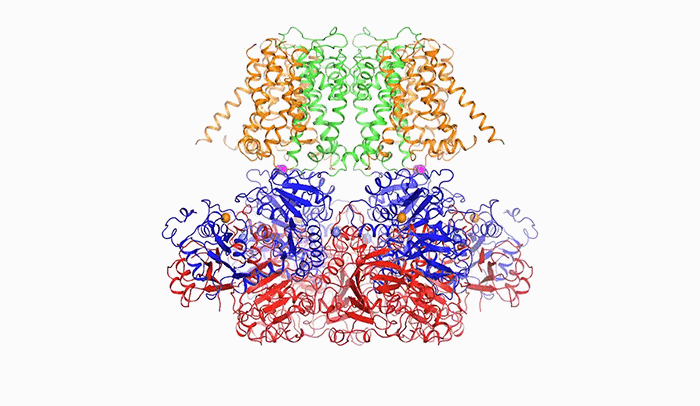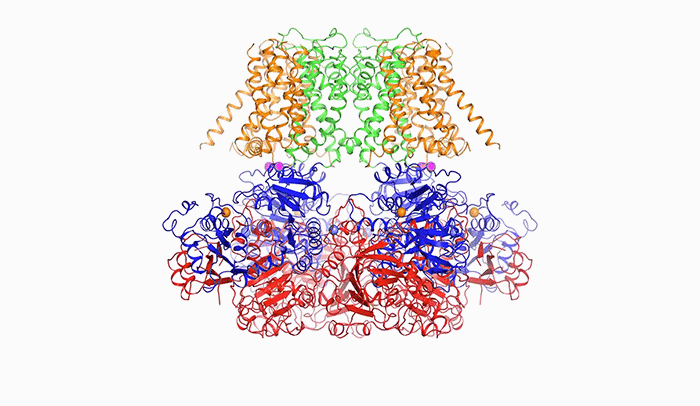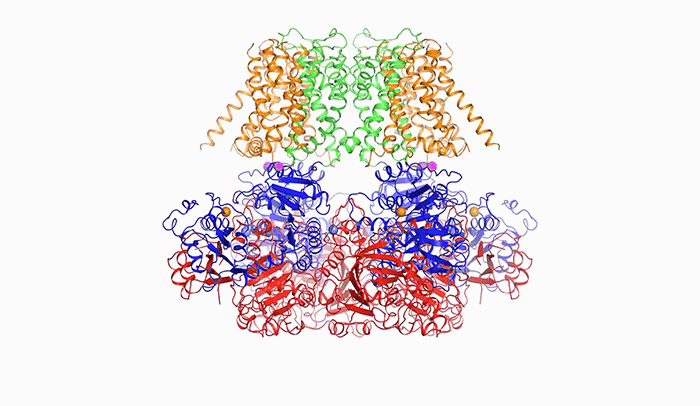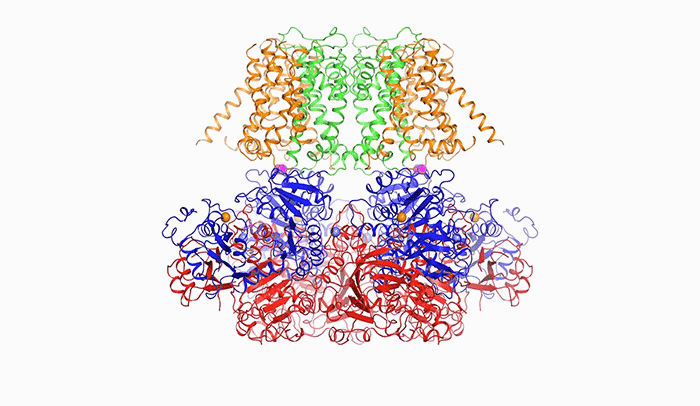







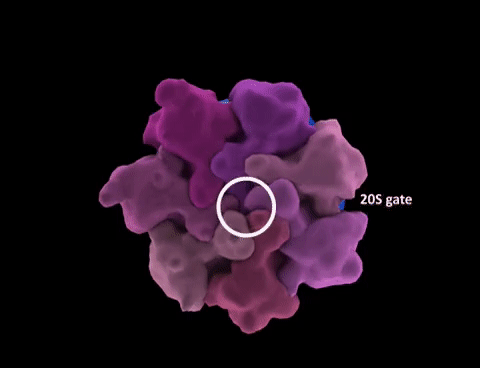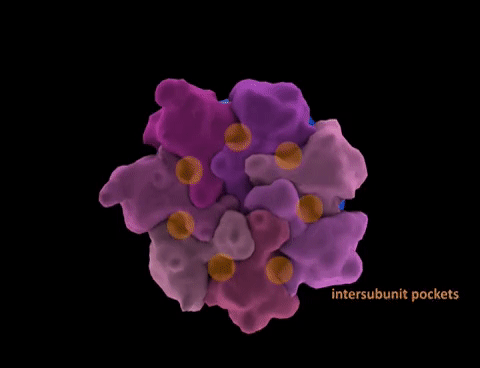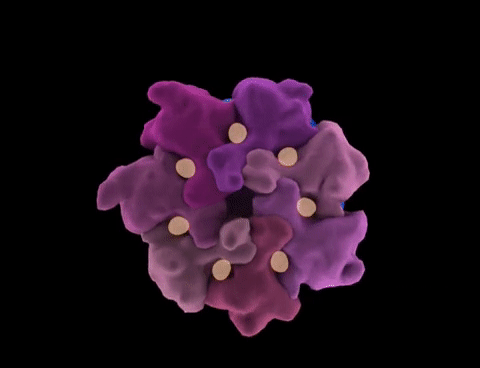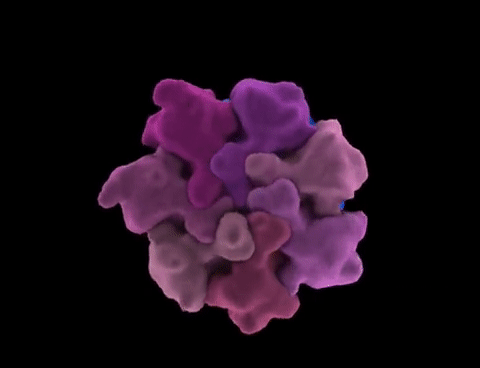


Genom można sobie wyobrazić, jako długi łańcuch złożony z 4 liter: A, C, T i G, podzielony na krótsze odcinki, które nazywamy genami. W genach zakodowane są białka:
Genom prokariotyczny i eukariotyczny:
Genom prokariotyczny:
Genom eukariotyczny:
Kod genetyczny i aminokwasy:
Aminokwasy budują białka:
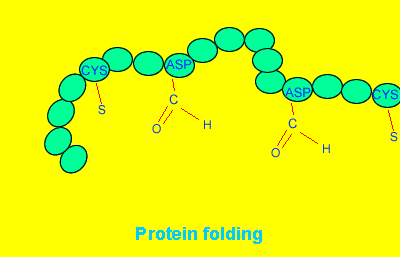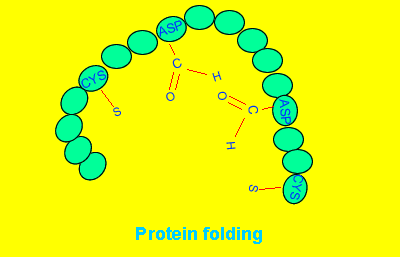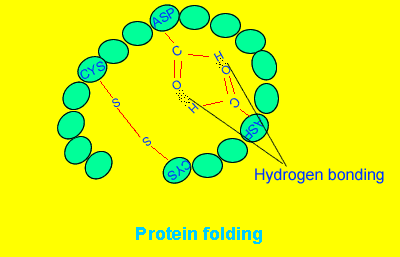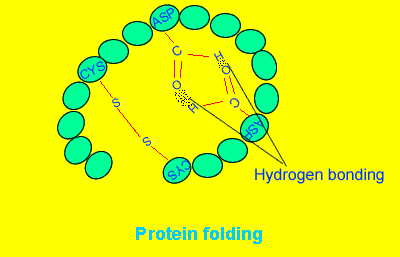
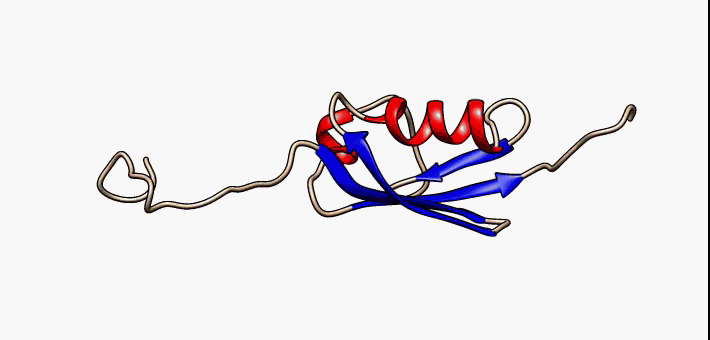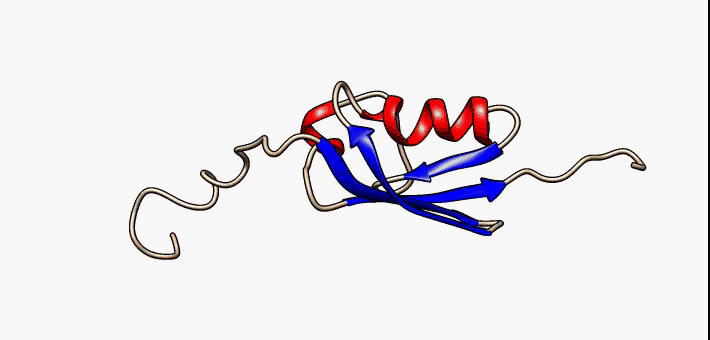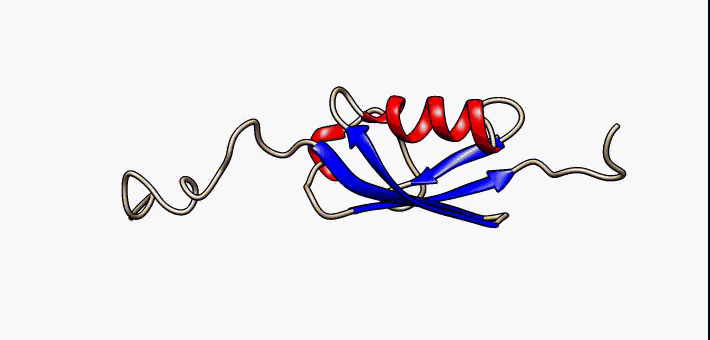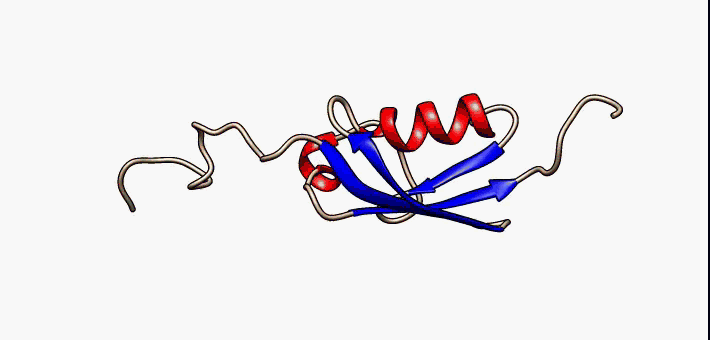
Białka to zwinięte łańcuchy – polipeptydy:
Często w zwijaniu polipeptydów pomagają inne białka (chaperony):

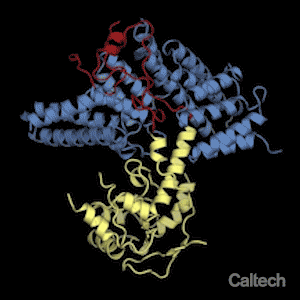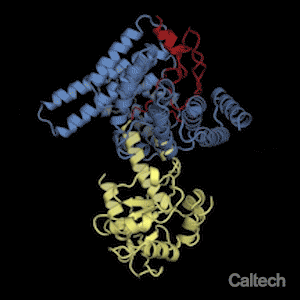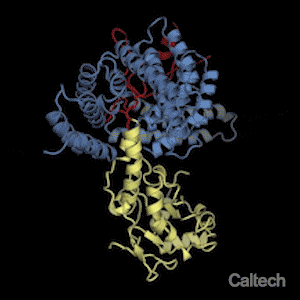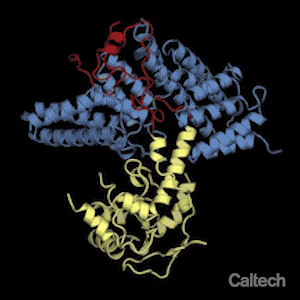
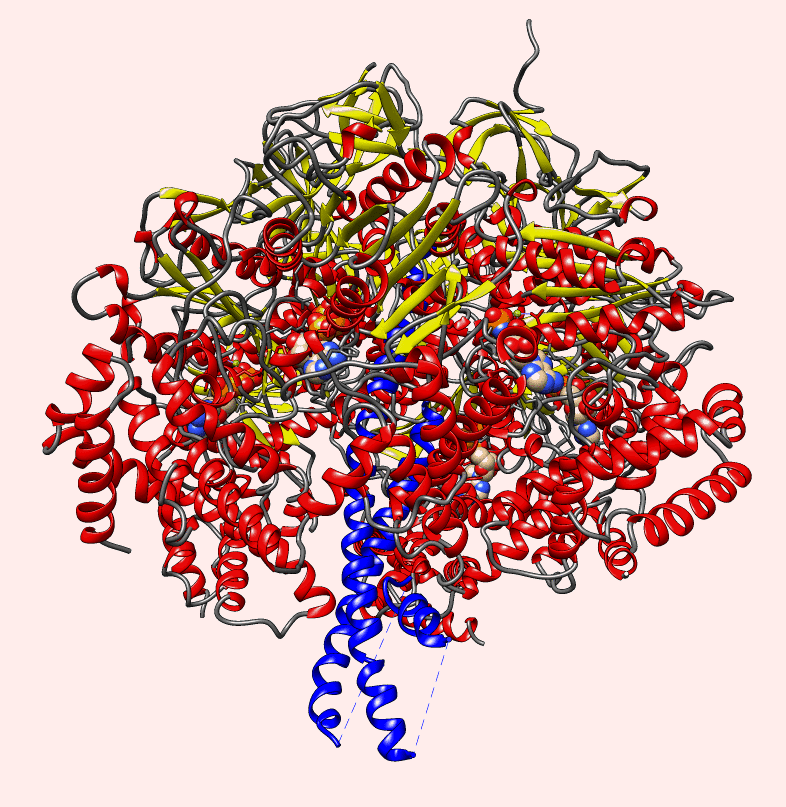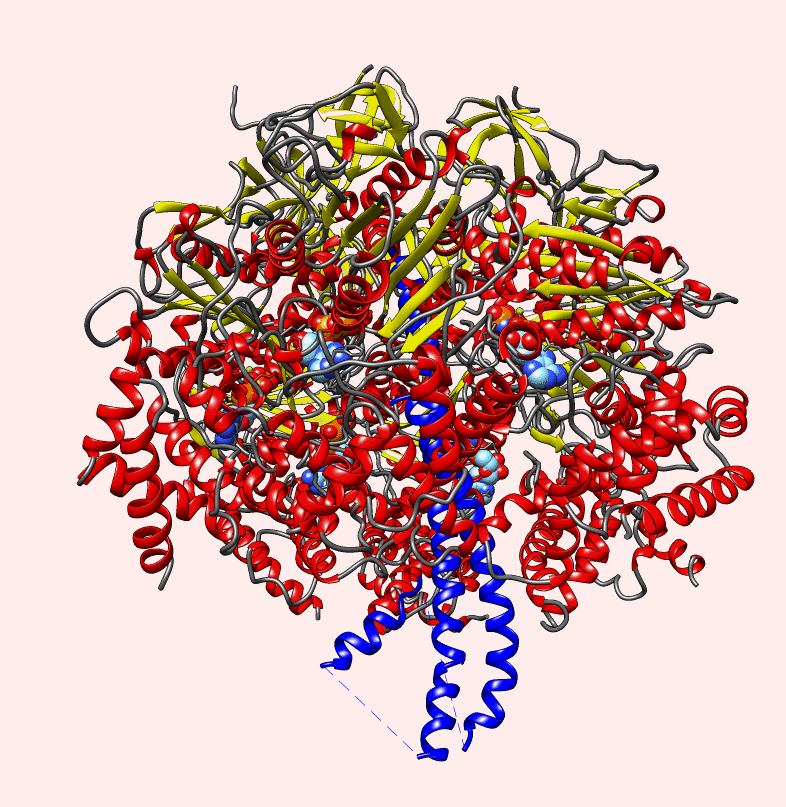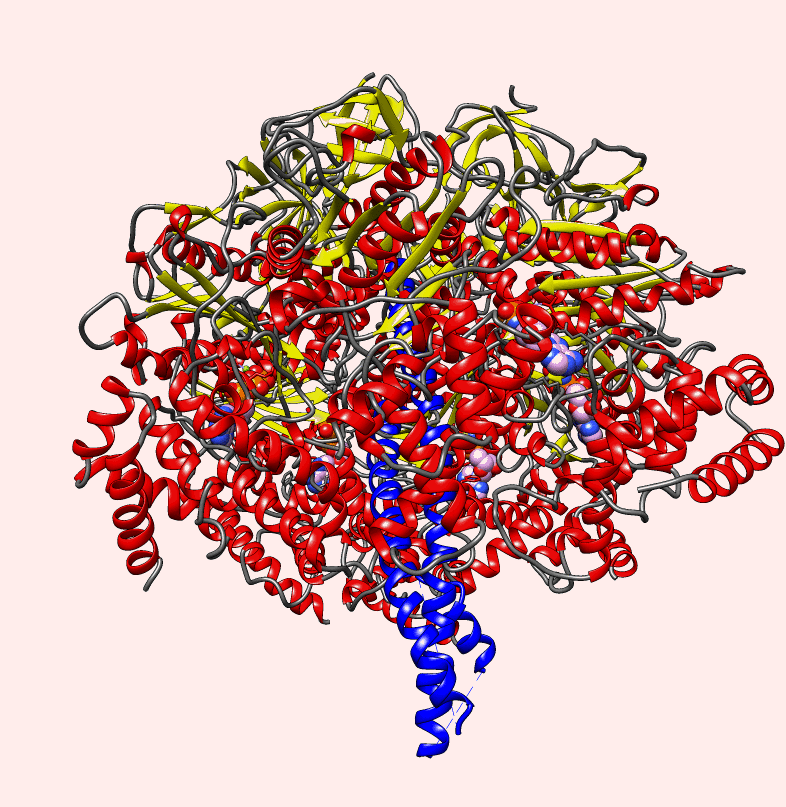
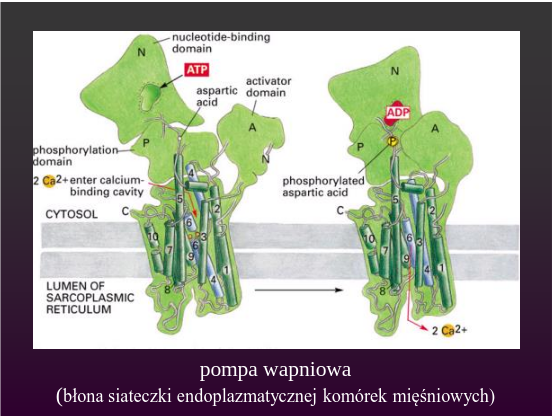
Białka zwijają się w najróżniejsze struktury przestrzenne, które pozwalają im na pełnienie różnych funkcji w komórce. Biolodzy strukturalni, to naukowcy zajmują się złożonymi kompleksami białkowymi. Takie systemy zbudowane są z osobnych, ściśle dopasowanych białek, które często są odpowiednikami elementów maszyn, podobnych do tych, jakie produkują ludzie. Jak widać na zamieszczonej animacji z takich klocków, które są pozwijanymi łańcuchami, zbudowana jest syntaza ATP, enzym który umożliwia życie każdemu organizmowi: od bakterii po człowieka, gdyż jest częścią większego kompleksu produkującego energię:




Do prawidłowego przebiegu tysięcy procesów, jakie zachodzą we wszystkich komórkach, jakie żyją na ziemi, od bakterii po te budujące nasze ciała, potrzebna jest energia zgromadzona w nukleotydach energetycznych. Najważniejszym z nich jest ATP. Nieustannie jest on rozkładany w komórkach do ADP i następnie z ADP powstaje na powrót ATP. Do syntezy ATP z ADP służy zintegrowany i nieredukowalnie złożony pod względem funkcji kompleks maszyn molekularnych, w tej czy innej (zmodyfikowanej) postaci istniejący u wszystkich organizmów żywych, który jest osadzony w błonie komórkowej, mitochondialnej czy plastydów:
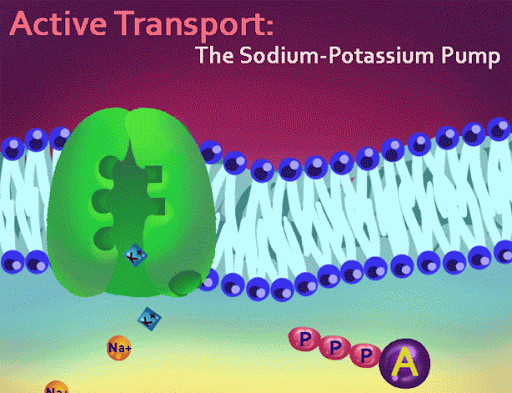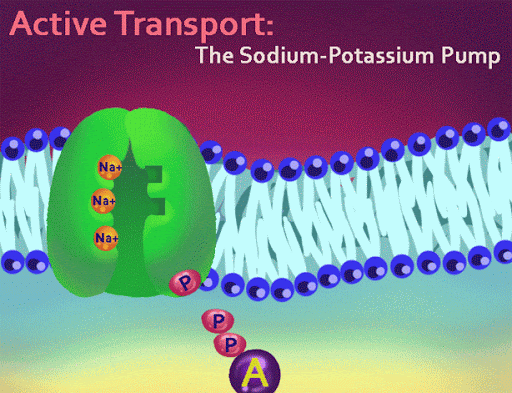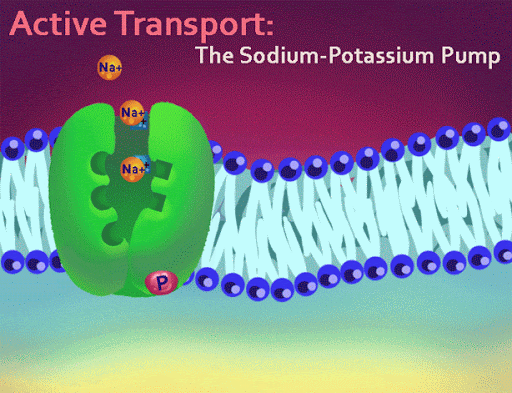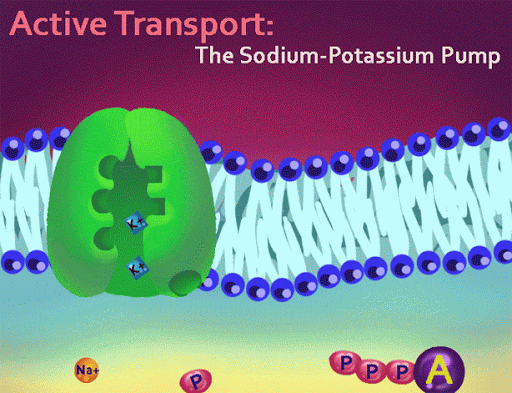


http://www.biotechnolog.pl/syntaza-atp
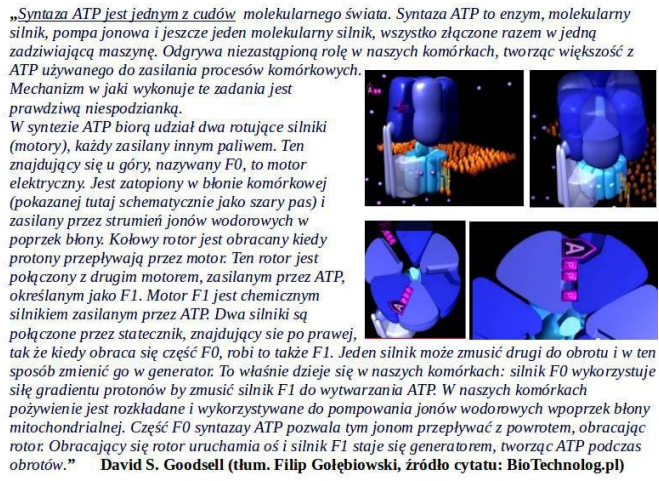
Rotujące motory
W syntezie ATP biorą udział dwa rotujące silniki (motory), każdy zasilany innym paliwem. Ten znajdujący się u góry, nazywany F0, to motor elektryczny. Jest zatopiony w błonie komórkowej (pokazanej tutaj schematycznie jako szary pas) i zasilany przez strumień jonów wodorowych w poprzek błony. Kołowy rotor jest obracany kiedy protony przepływają przez motor:

Cała ta konstrukcja składa się z pozwijanych łańcuchów (polipeptydów):

Ten rotor jest połączony z drugim motorem, zasilanym przez ATP, określanym jako F1. Motor F1 jest chemicznym silnikiem zasilanym przez ATP. Syntaza ATP może pracować w obu kierunkach: syntetyzując ATP z ADP i hydrolizując (rozkładając) ATP do ADP:


https://j.p.gogarten.uconn.edu/mcb3421_2019/labs/assign2.html

https://www6.slac.stanford.edu/file/rotaryprotonsvpumpanimfinalgif

Cukry:
Lipidy (tłuszcze):
Jeszcze trochę o białkach. Białka to przeciwciała, enzymy, hormony, białka strukturalne oraz transportujące.
Enzymy pełnią funkcję katalizatorów, przyśpieszając reakcje chemiczne, na przykład zachodzące podczas trawienia. Właściwie. Bez enzymów szybko umarlibyśmy z głodu, ponieważ strawienie zwykłego posiłku byłoby niemożliwe. Enzymy działają jak na linii produkcyjnej, każdy z nich wykonuje określone zadanie:
Kompleks dehydrogenazy – Super animacja!
https://pl.wikipedia.org/wiki/Dehydrogenazy
„Dehydrogenazy – ogólna nazwa grupy enzymów zaliczanych do oksydoreduktaz, odczepiających atomy wodoru (łac. hydrogenium) z rozmaitych związków organicznych występujących w organizmach żywych. Przykładem może być kompleks dehydrogenazy kwasów tłuszczowych czy enzymy cyklu Krebsa. „

Niektóre białka to hormony, działające jako posłańcy. Wydzielane do krwiobiegu, stymulują albo hamują aktywność różnych części organizmu. Na przykład insulina pobudza komórki do wchłaniania glukozy, będącej ich źródłem energii:
Białka strukturalne, takie jak kolagen i keratyna, są głównym składnikiem chrząstki, włosów, paznokci i skóry:
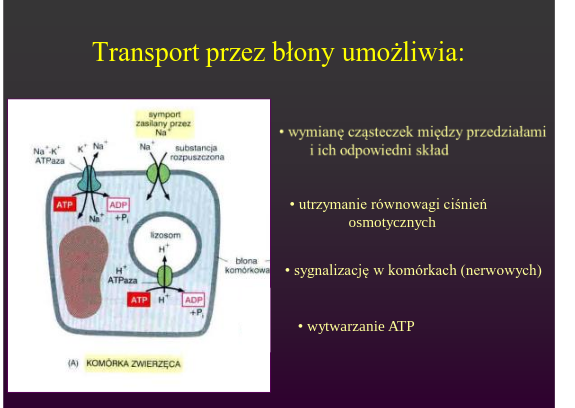
Transport przez błony
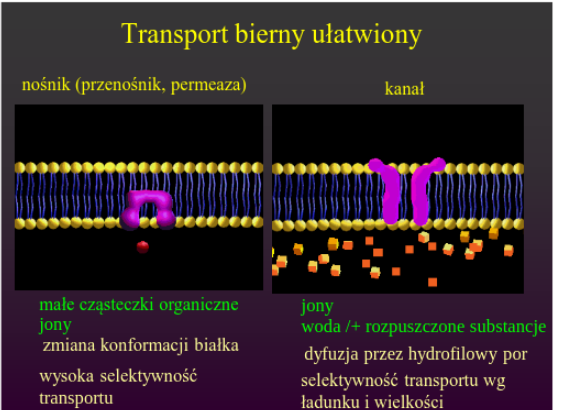
Białka transportujące, które znajdują się w błonach komórkowych, działają niczym pompy i tunele. Wpuszczają do komórek i wypuszczają różne substancje:





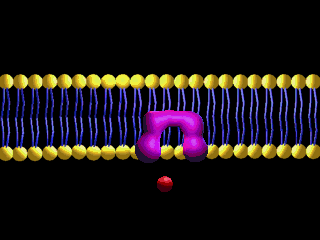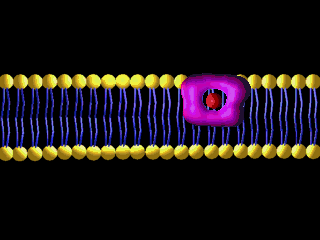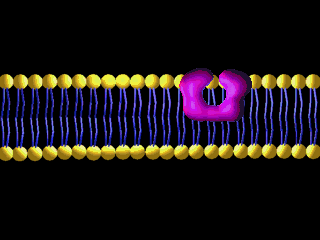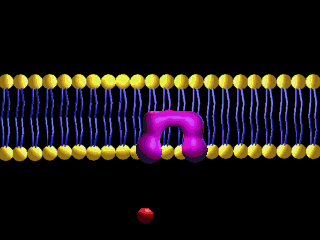





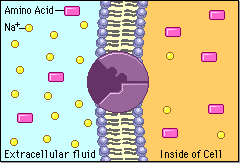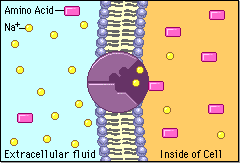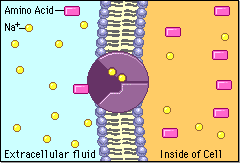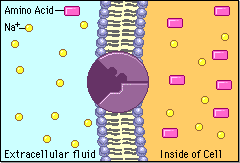



http://nklia.wordpress.com/opracowania/budowa-i-dzialanie-narzadu-sluchu/
„W procesie słyszenia zachodzą cztery przekształcenia energii (Gerrig & Zimbardo, 2009).
Na początku, docierająca do małżowiny usznej fala dźwiękowa (akustyczna, czyli drgające cząsteczki powietrza) zostaje przekształcona w energię mechaniczną dzięki współpracy błony bębenkowej i kosteczek słuchowych. Część bodźca dźwiękowego dociera bezpośrednio do zewnętrznego przewodu słuchowego, część natomiast jest odbita od małżowiny usznej. Kierunek odbić dochodzących do niej fal zależny jest od jej ukształtowania i wspomaga lokalizację źródła dźwięku. Drgania przenoszą się wzdłuż ucha zewnętrznego, aż do błony bębenkowej. Dzięki zmianie ciśnienia jest ona wprawiana w ruch i przekazuje fale do ucha środkowego. Młoteczek, kowadełko i strzemiączko skupiają drgania i przekazują je dalej – do okienka owalnego ślimaka. Dzięki temu, że powierzchnia błony bębenkowej jest około 20 razy większa od podstawy strzemiączka, niewielkie jej wibracje powodują silne drgania kosteczek (Kalat, 2006). Następna przemiana zachodzi w uchu wewnętrznym. Do okienka owalnego ślimaka strzemiączko przekazuje drgania, co wywiera na nie nacisk, a w efekcie zmniejsza się bądź zwiększa ciśnienie wewnątrz przewodu ślimakowego. Znajdujący się w ślimaku płyn pobudza i wprawia w ruch błonę podstawną ślimaka, która rozciągnięta jest na całej jego długości. Dźwięki o niskiej częstotliwości (poniżej 500 Hz) pobudzają komórki blisko wierzchołka ślimaka, o wysokiej natomiast (powyżej 10000 Hz) – blisko podstawy, w początkowym odcinku (Sadowski, 2001).
Kolejne przekształcenie wywołane jest ruchami błony podstawnej, które powodują wyginanie się komórek rzęsatych połączonych z błoną. Zmysłowe komórki rzęsate narządu Cortiego przetwarzają bodźce mechaniczne drgań endolimfy, które zostały wywołane falami akustycznymi, na zmianę potencjału elektrycznego swojej błony komórkowej. W efekcie polaryzacji pobudzone zostają komórki nerwowe przylegające do komórek rzęsatych a impulsy nerwowe biegną do odpowiednich ośrodków słuchowych w mózgu.”
(2) Filament (złożony z białek sznur), który łączy „drzwiczki” mechanoreceptora z elementem, który odchylając się w przeciwną do tych „drzwiczek” stronę ciągnie na filament (białkowy sznurek) i otwiera mechanoreceptor – to odginanie następuje pod ciśnieniem napływających do ucha wewnętrznego fal dźwiękowych. Uginają się pod wpływem fal dźwiękowych, jak drzewa podczas silnego wiatru:


„Kanały aktywowane naprężeniem mechanicznym (mechanoreceptory) ulegają otwarciu w odpowiedzi na pojawienie się w błonie sił odkształcających ją (naprężeń). Ta ich właściwość powoduje, że są one wykorzystywane w komórkach dokonujących zamiany sygnałów mechanicznych na elektryczne. Typowym przykładem są tu komórki rzęsate znajdujące się w błonie podstawnej w narządzie Cortiego, przetwarzające dźwięki na impulsy elektryczne.”





https://pl.wikipedia.org/wiki/Receptor_GABA
„Receptory GABA – rodzaje receptorów błonowych wiążących kwas γ-aminomasłowy (GABA), pełniących ważną rolę w funkcjonowaniu układu nerwowego. Receptory te dzielą się na trzy klasy: GABAA (receptor jonotropowy), GABAB (powiązany z białkiem G receptor metabotropowy) i zidentyfikowany później GABAC (receptor jonotropowy)
Receptor GABAA
Receptor ten stanowi kanał chlorkowy zbudowany z pięciu podjednostek białkowych. Jego aktywność regulowana jest wiązaniem swoistego liganda – kwasu γ-aminomasłowego. Związek ten powoduje aktywację receptora i otwarcie kanału jonowego, co z kolei skutkuje zwiększeniem napływu jonów chlorkowych do wnętrza komórki. W związku z tym, że receptory te znajdują się w błonie komórkowej neuronów, napływ jonów Cl– powoduje wzrost różnicy potencjałów po obu stronach błony, czyli jej hiperpolaryzację. W efekcie utrudnione zostaje powstawanie potencjałów czynnościowych odpowiadających za przekazywanie informacji w układzie nerwowym. Z tego powodu GABA nazywany jest aminokwasem hamującym, a jego receptor receptorem hamującym.
Receptor GABAA oprócz miejsca wiążącego GABA, zawiera również domeny rozpoznające barbiturany, benzodiazepiny, kwas walerenowy, pikrotoksynę, alkohole i anestetyki. Miejsca te niekiedy określane są jako samodzielne receptory (np. receptor benzodiazepinowy).
Cukier może zrewolucjonizować biologię w nie mniejszym stopniu niż odkrycie DNA!
Receptor GABAB
W odróżnieniu od poprzedniego receptora, GABAB jest receptorem metabotropowym, powiązanym poprzez białko G z kanałem potasowym i wapniowym, jak również z cyklazą adenylową i fosfolipazą C. Zlokalizowane na presynaptycznych zakończeniach nerwowych, pełnią funkcję tak autoreceptorów, jak i heteroreceptorów, regulując uwalnianie neuroprzekaźników. Agonistą tych receptorów jest baklofen, lek zwiotczający mięśnie szkieletowe. Pobudzenie receptora GABAB skutkuje powolnym i przedłużonym zahamowaniem uwalniania neuroprzekaźników.”
Ostatnimi czasy naukowcy badają, jak komórki wykorzystują cukry proste, na przykład glukozę, do budowania gigantycznych molekuł, „które wielkością i złożonością konkurują z DNA i proteinami” — informuje czasopismo New Scientist. „Cukry uczestniczą niemalże w każdym procesie biologicznym — począwszy od rozpoznawania patogenów poprzez krzepnięcie krwi aż po umożliwianie plemnikom wniknięcia do jaja”. Zarazem w nieprawidłowej syntezie cukrów upatruje się przyczyn rosnącej liczby chorób, takich jak dystrofia mięśniowa czy reumatoidalne zapalenie stawów. W raporcie czytamy: „Biolodzy dopiero zaczynają pojmować działanie cukrów i dlatego muszą na nowo przeanalizować długo uznawane poglądy na temat funkcjonowania procesów życiowych”.
W odniesieniu do pełnego zestawu cukrów komórki lub organizmu naukowcy ukuli termin „glikom”, przez analogię do terminu „genom”, obejmującego pełny zestaw genów. Ale glikom komórki jest „prawdopodobnie tysiące razy bardziej skomplikowany niż genom” — uważa Ajit Varki, dyrektor Ośrodka Badawczo-Szkoleniowego Glikobiologii na Uniwersytecie Kalifornijskim w San Diego w USA. Dlaczego glikom jest aż tak złożony?
W komórkach cukry proste (monosacharydy) wiążą się i tworzą wielocukry (polisacharydy). Te z kolei są zgrupowane w gigantyczne molekuły, które mogą zawierać ponad 200 jednostek cukrowych. Ponieważ cukry proste mają strukturę trójwymiarową, kluczową dla ich funkcjonowania, „cząsteczka cukru złożona zaledwie z sześciu jednostek potencjalnie ma możliwość tworzenia zawrotnej liczby 12 miliardów konfiguracji” — podaje New Scientist.
Opisując trudne zadania, przed którymi stoją badacze rozwijającej się dziedziny nauki nazywanej glikobiologią, Ajit Varki oświadczył: „To tak, jakbyśmy dopiero co odkryli kontynent Ameryki Północnej. Musimy teraz wysłać zwiadowców, żeby się przekonać, jak duży zajmuje obszar”.

Tłuszcze, lipidy

Pory jądrowe:
Transport bierny:
Transport pęcherzykowy:
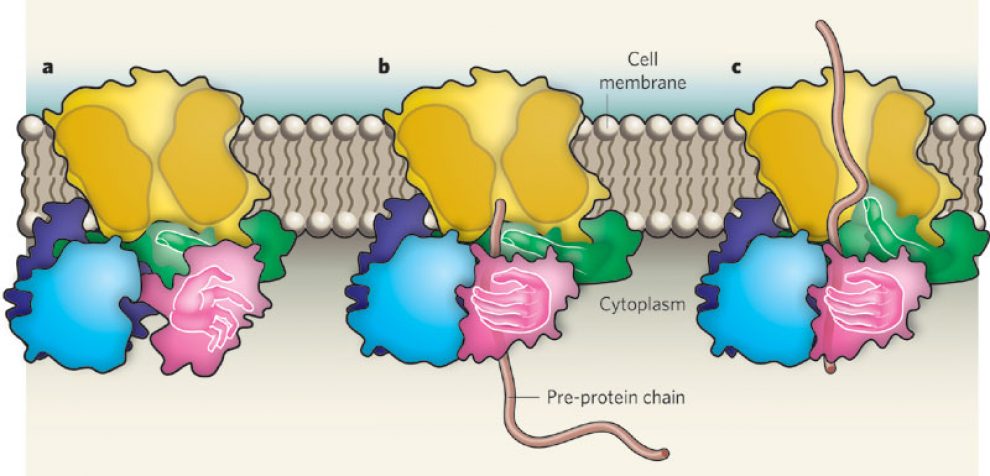
Znamy już pierwszych w tym roku laureatów prestiżowej Nagrody Nobla. Przyznawanie tego tytułu rozpoczęto od medycyny i fizjologii. Nagrodzeni zostali trzej badacze: James E. Rothman z Yale University, Randy W. Schekman z Uniwersity of California i Thomas C. Südhof ze Stanford University. W ten sposób doceniono ich badania nad mechanizmem regulującym główny system transportowy w naszych komórkach.
W oficjalnym komunikacie komisji przyznającej Nagrody nobla możemy znaleźć informację, że wspomniani naukowcy otrzymali nagrodę „za odkrycie mechanizmu regulującego transport pęcherzykowy, główny system transportu w naszych komórkach”. Ale co się za tym kryje?
Pęcherzyki, o których mowa, znajdują się we wnętrzu komórek, a ich zawartość oddzielona jest od otoczenia warstwą lipidową. W ich wnętrzu, na skutek działania przeróżnych mechanizmów, są przechowywane, transportowane, modyfikowane, wydzielane i wchłanianie substancje uczestniczące w procesach zachodzących we wnętrzu żywych komórek. Odpowiednie pęcherzyki są podstawą organizacji transportu komórkowego. Transport pęcherzykowy, bo o nim mowa, zapewnia również możliwość sortowania substancji w zależności od miejsca, do którego mają dotrzeć. Jest on również narzędziem, dzięki któremu możliwa jest komunikacja pomiędzy różnymi organellami znajdującymi się w środku komórki.
Każdy z trzech laureatów tegorocznej Nagrody Nobla z medycyny i fizjologii odkrył inny element mechanizmu odpowiadającego za tworzenie i odpowiednie rozprzestrzenianie pęcherzyków. [….]
Inny rodzaj transportu pęcherzykowego, który nie jest zależny od klatryny:
Polecam:
To, czego dziś się dowiedzieliście zawdzięczamy ciężkiej pracy takich biologów. Ten poświęcił życie i karierę, żeby zbadać i opisać ten proces!
W pełni zasłużone laury!
Źródła:
https://www.sdbonline.org/sites/fly/lewhelddeep/deephomology11.htm
Comparative Analysis of Gene Expression for Convergent Evolution of Camera Eye Between Octopus and Human
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC509264/
Comparative Analysis of Gene Expression for Convergent Evolution of Camera Eye Between Octopus and Human
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC509264/
Reszta w niniejszym tekście oraz w innych moich opracowaniach, które podlinkowałem 🙂

























































Musisz się zalogować aby dodać komentarz.